Окислительная атака на белки модифицирует остатки аминокислот, фрагментирует пептидные цепи, приводит к сшивке белков, изменяет заряд белка и его чувствительность к протеолизу.
В белках наиболее уязвимыми к повреждающему действию свободных радикалов оказываются серусодержащие аминокислоты, остатки лизина, триптофана и гистидина. Окислительное разрушение белка усиливается в присутствии металлов, способных отдавать электроны, например, ионов Fe2+. Присутствие металла позволяет локально образовывать гидроксил-радикал в реакции Фентона и окислять аминокислотные остатки в непосредственной близости от него.
Активные радикалы (АФК, хлорамины) способны отрывать атом водорода от тиольной группы цистеина, формируя тиольные радикалы и дисульфидные сшивки между белками. В качестве примеров повреждения белков свободными радикалами можно привести окисление SH-групп цистеина и образование сульфоксида метионина.
Окисление серусодержащих групп цистеина и метионина

Окисление метионина до сульфоксида
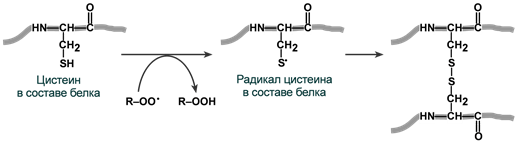
Окисление и неферментативная димеризация цистеина
Образование хлораминов
Образуемый миелопероксидазой гипохлорит-ион (OCl–) по силе воздействия сопоставим с гидроксил-радикалом, и он атакует аминогруппы остатков лизина в белках с образованием структур хлораминов.
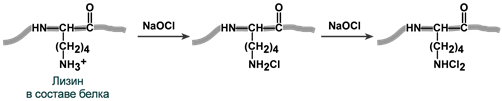
Схема окисления лизина и образование хлораминов
Хотя хлорамины сами по себе нарушают функционирование микробных белков, главный бактерицидный эффект гипохлорит-иона обусловлен дальнейшим отщеплением хлораминовой группы, окислением δ-углеродного атома лизина до альдегидной группы и появлением новой аминокислоты аллизина. Аналогичным эффектом на лизин в белках обладают гидроксил-радикалы и пероксинитрит-ион.
