Ферменты, ликвидирующие АФК
1. Супероксиддисмутаза (СОД) – фермент, представленный в цитозоле и митохондриях, выполняет функции антиоксидантного фермента, удаляя агрессивный супероксид анион-радикал и образуя при этом более устойчивый пероксид водорода.
У человека имеется три формы фермента:
- цитозольная и внеклеточная формы, содержат металлы медь и цинк,
- митохондриальный изофермент, включает марганец.

Реакция, катализируемая супероксиддисмутазой
2. Каталаза, гемсодержащий фермент, присутствует в пероксисомах всех клеток человека и обладает чрезвычайно высокой молекулярной активностью. В эритроцитах она находится в цитозоле и защищает гемоглобин от окисления.

Реакция, катализируемая каталазой
3. Глутатионпероксидаза, как и каталаза, является гемсодержащим ферментом и обезвреживает H2O2. Обладая в 1000 раз большим сродством к пероксиду водорода, чем каталаза, она эффективна даже при низких его концентрациях.
Особенностью глутатионпероксидазы является наличие в активном центре фермента селеноцистеина, т.е. такого цистеина, в котором сера заменена на селен.
В качестве восстановителя для H2O2 фермент использует трипептид глутатион, содержащий цистеин с его SH-группой. Окисленный в результате реакции глутатион восстанавливается глутатионредуктазой.
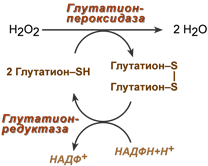
Реакция, катализируемая глутатионпероксидазой
4. Глутатион-S-трансфераза обеспечивает взаимодействие различных веществ с восстановленным глутатионом. Существуют три вида фермента – митохондриальный, микросомальный и цитозольный (у млекопитающих до 10% всех белков цитоплазмы). Мишенью фермента являются различные ксенобиотики и пероксиды липидов (но не H2O2). При реакции восстановленного глутатиона с перекисью жирной кислоты происходит восстановление окисленной группы до спирта и воды.
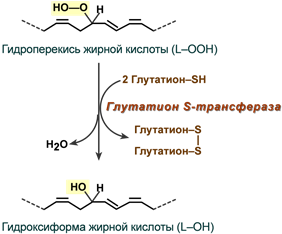
Антиоксидантная реакция, катализируемая глутатион-S-трансферазой
4. Пероксиредоксины – антиоксидантные ферменты, контролирующие уровень цитокин-индуцированных пероксидов, участвующих в передаче клеточных сигналов.
В активном центре фермента находятся SH-группы цистеина, которые окисляются до R-SOH состояния пероксидным субстратом (H2O2 или липидной гидроперекисью)
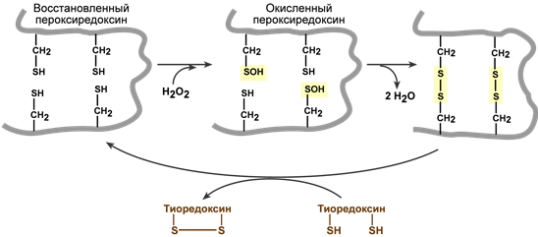
Роль пероксиредоксинов в нейтрализации пероксида водорода
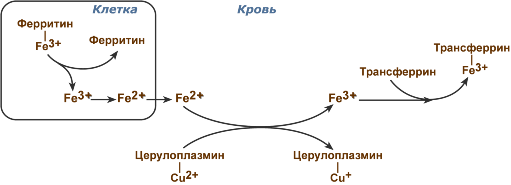
5. Церулоплазмин – антиоксидантный фермент плазмы крови, содержит 6-8 ионов меди (II) и окисляет ионы Fe2+ до Fe3+ без образования гидроксил-радикала (сравните с реакцией Фентона). Ион железа (III) далее связывается с белком трансферрином. Таким образом, церулоплазмин обеспечивает равновесие между депонированием и использованием железа, а применительно к СРО препятствует инициации свободнорадикальных процессов.