Так как синтез и окисление глюкозы являются крайне важными для существования клетки (гликолиз) и всего организма (глюконеогенез), то регуляция этих процессов отвечает запросам органов и тканей при различных условиях.
Поскольку гликолитическое окисление глюкозы
- является способом получения энергии в аэробных и анаэробных условиях, то оно непрерывно происходит во всех клетках и, конечно, должно и будет активировано при усилении работы клетки, например, сокращение миоцита, движение нейтрофилов;
- служит источником глицерола и ацетил-SКоА, используемых для синтеза жиров в гепатоцитах и адипоцитах, то такое окисление активируется при избытке глюкозы в этих клетках.
Глюконеогенез, как образование глюкозы в печени из неуглеводных источников, необходим:
- при гипогликемии во время мышечной нагрузки – синтез глюкозы из молочной кислоты, поступающей из работающих мышц, и из глицерола, образующегося при мобилизации жиров;
- при гипогликемии при кратком голодании (до 24 часов) – синтез преимущественно из молочной кислоты, непрерывно поступающей в печень из эритроцитов,
- при гипогликемии при длительном голодании – в основном синтез из аминокислот, образующихся при катаболизме белков, и также из молочной кислоты и глицерина.
Таким образом, глюконеогенез, идущий в печени, обеспечивает глюкозой все остальные клетки и органы (эритроциты, нервная ткань, мышцы и др.), в которых активны процессы, требующие глюкозу. Поступление глюкозы в эти клетки также необходимо, чтобы поддержать концентрацию оксалоацетата и обеспечить сгорание в ЦТК ацетил-SКоА, получаемого из жирных кислот или кетоновых тел.
В целом можно выделить два способа регуляции гликолиза и глюконеогенеза: гормональная при участии гормонов и метаболическая, т.е. при помощи промежуточных или конечных продуктов обмена глюкозы.
Существуют три основных участка, на которых происходит регуляция этих процессов:
- первая реакция гликолиза,
- третья реакция гликолиза и обратимая ей,
- десятая реакция гликолиза и обратимые ей.
Регуляция глюконеогенеза
Гормональная активация глюконеогенеза осуществляется глюкокортикоидами, которые увеличивают синтез пируваткарбоксилазы, фосфоенолпируват-карбоксикиназы, фруктозо-1,6-дифосфатазы.
Глюкагон стимулирует те же самые ферменты через аденилатциклазный механизм путем фосфорилирования.
Энергия для глюконеогенеза поступает от β-окисления жирных кислот. Конечный продукт этого окисления, ацетил-SКоА аллостерически стимулирует активность первого фермента глюконеогенеза – пируваткарбоксилазы. Кроме этого, фруктозо-1,6-дифосфатаза стимулируется при участии АТФ.
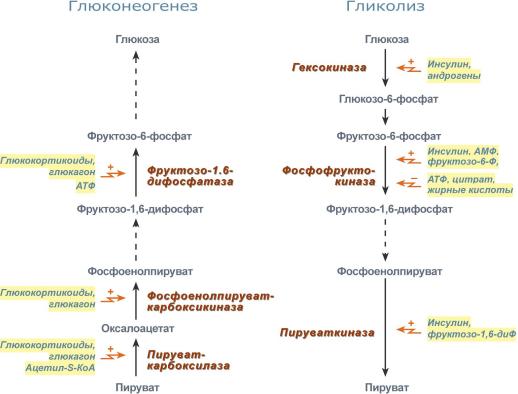
Гормональные и метаболические факторы, регулирующие гликолиз и глюконеогенез
Регуляция гликолиза
Гормональная регуляция
В печени гликолиз стимулируется инсулином, повышающим количество ключевых ферментов гликолиза (гексокиназы, фосфофруктокиназы, пируваткиназы).
В печени активность глюкокиназы, кроме инсулина, регулируется другими гормонами:
- активацию вызывает андрогены,
- подавляют ее активность глюкокортикоиды и эстрогены.
В других тканях активность гексокиназ
- повышается тиреоидными гормонами,
- снижается – глюкокортикоидами и соматотропином.
Метаболическая регуляция
Гексокиназа непеченочных клеток ингибируется продуктом собственной реакции – глюкозо-6-фосфатом.
Фосфофруктокиназа:
- активируется АМФ и собственным субстратом (фруктозо-6-фосфат),
- ингибируется – АТФ, лимонной кислотой, жирными кислотами.
Пируваткиназа активируется фруктозо-1,6-дифосфатом (прямая положительная регуляция).
Молекулы АМФ, стимулирующие гликолиз, образуются в аденилаткиназной реакции, активируемой при появлении избытка АДФ. Особенно ярко значение такой регуляции проявляется при мышечной работе:
АДФ + АДФ ↔ АТФ + АМФ
